- Autorius Alex Aldridge aldridge@what-difference.com.
- Public 2023-12-17 13:44.
- Paskutinį kartą keistas 2025-06-01 07:37.
Pagrindinis skirtumas - alifatiniai ir aromatiniai angliavandeniliai
Pirmiausia trumpai pažiūrėkime, kokie angliavandeniliai kalba apie skirtumą tarp alifatinių ir aromatinių angliavandenilių. Angliavandeniliai yra organiniai junginiai, kurių struktūroje yra anglies ir vandenilio atomų. Pagrindinis skirtumas tarp alifatinių ir aromatinių angliavandenilių yra tas, kad alifatiniuose angliavandeniliuose nėra konjuguotos jungčių sistemos, tuo tarpu aromatiniuose angliavandeniliuose yra konjuguotų jungčių sistema. Tačiau abi šios molekulės laikomos organiniais junginiais.
Kas yra alifatiniai angliavandeniliai?
Alifatiniai angliavandeniliai yra organinės molekulės, kurių struktūroje yra anglies (C) ir vandenilio (H) atomų; tiesiomis grandinėmis, šakotomis grandinėmis arba nearomatiniais žiedais. Alifatiniai angliavandeniliai gali būti suskirstyti į tris pagrindines grupes; alkanai, alkenai ir alkinai.
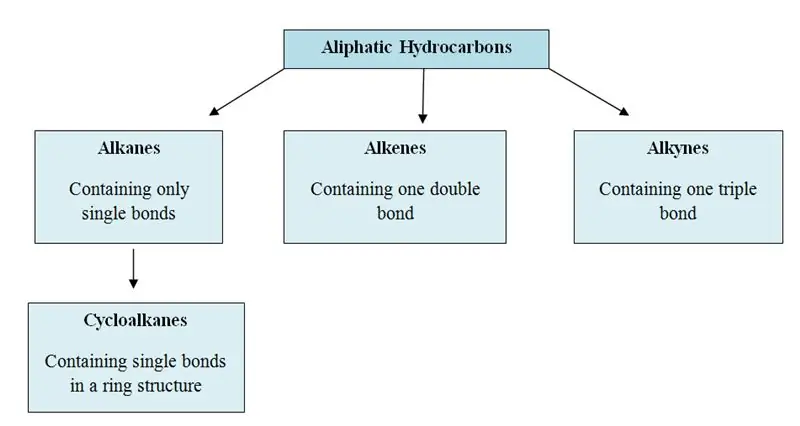
Kas yra aromatiniai angliavandeniliai?
Aromatiniai angliavandeniliai kartais žinomi kaip „arenai“arba „ariliniai angliavandeniliai“. Daugumos aromatinių angliavandenilių struktūroje yra benzeno žiedas; tačiau yra nebenzeno aromatinių angliavandenilių, vadinamų heteroarenais, kurie laikosi „Haklio taisyklės“(cikliniai žiedai, kurie laikosi Haklio taisyklės, turi 4n+2 π-elektronų skaičių; kur n=0, 1, 2, 3, 4, 5, 6). Kai kurie aromatiniai angliavandeniliai turi daugiau nei vieną žiedą; jie vadinami policikliniais aromatiniais angliavandeniliais.
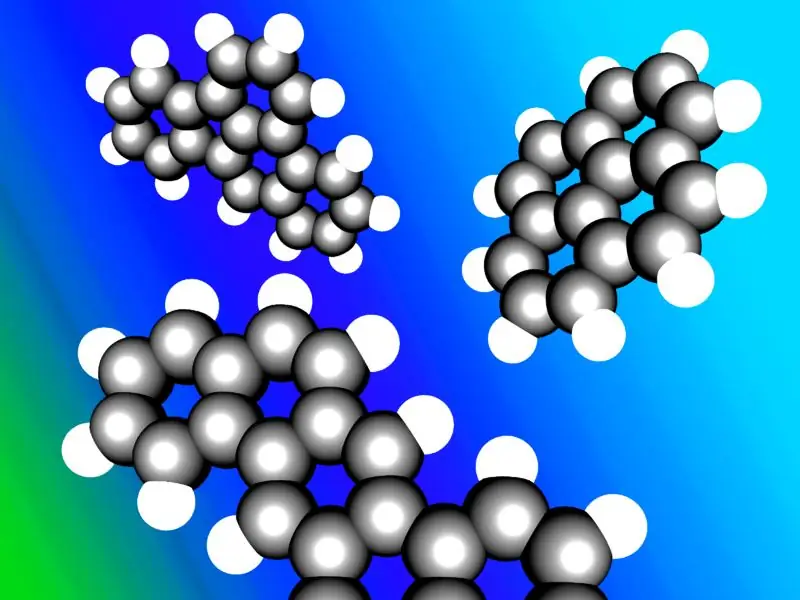
Tipinių policiklinių aromatinių angliavandenilių iliustracija.
Kuo skiriasi alifatiniai ir aromatiniai angliavandeniliai?
Alifatinių ir aromatinių angliavandenilių struktūra
Alifatiniai angliavandeniliai: jų struktūroje yra tiesios grandinės, šakotos grandinės arba nearomatiniai žiedai. Ši grupė turi ir sočiųjų, ir nesočiųjų angliavandenilių. Alkanai yra sotieji angliavandeniliai, alkenai ir alkinai yra nesotieji angliavandeniliai.
Tiesios grandinės:
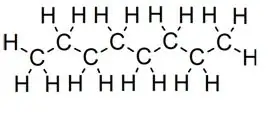
Oktanas
Firminės grandinės:
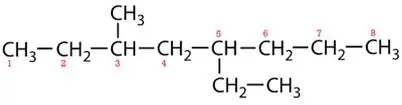
5-etil-3-metiloktanas

2-metil-3-pentencija
Nearomatiniai žiedai:
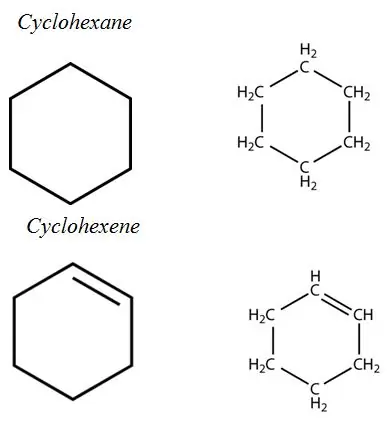
Aromatiniai angliavandeniliai: aromatinių angliavandenilių struktūroje yra aromatinių žiedų sistema. Visi jie yra nesotieji angliavandeniliai, bet gana stabilūs dėl konjuguotų ryšių sistemos.
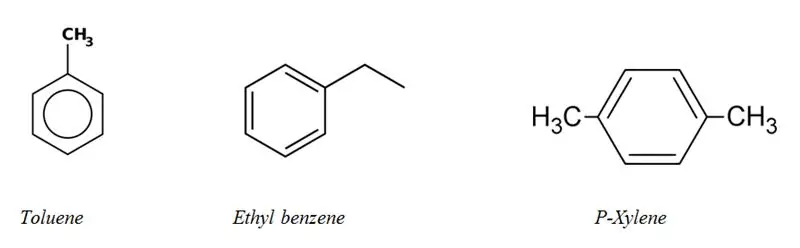
Alifatinių ir aromatinių angliavandenilių kategorijos
Alifatiniai angliavandeniliai:
Alifatiniuose angliavandeniliuose yra trys pagrindinės grupės; alkanai, alkenai ir alkinai. Jie taip pat žinomi kaip alilo angliavandeniliai.
Alkanai: alkanuose anglies ir vandenilio atomai yra sujungti viengubomis jungtimis. Jie neturi kelių obligacijų. Alkanai sudaro žiedines struktūras, jie vadinami cikloalkanais.
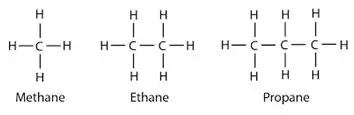
Alkenai: Šioje grupėje yra ir viengubos, ir dvigubos jungtys tarp anglies atomų. Vandenilio ir anglies atomai visada sudaro pavienes jungtis.
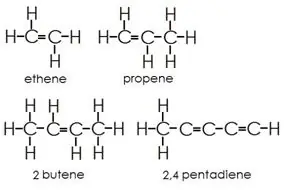
Alkinai: be pavienių jungčių, alkinai turi ir trigubus anglies atomų ryšius.
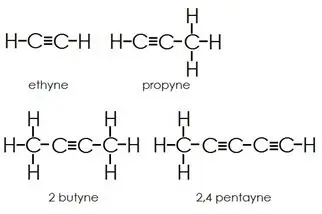
Aromatiniai angliavandeniliai:
Daugelio aromatinių angliavandenilių struktūroje yra bent vienas benzeno žiedas. Tačiau nebenzeno aromatinių angliavandenilių yra nedaug, jie vadinami „heteroarenais“. Aromatiniai angliavandeniliai vadinami „ariliniais“angliavandeniliais.
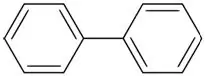
Bifenilas (aromatinis angliavandenilis su dviem benzeno žiedais)
Alifatinių ir aromatinių angliavandenilių sujungimo modelis
Alifatiniai angliavandeniliai:
Alifatiniuose angliavandeniliuose; viengubos, dvigubos ar trigubos jungtys gali egzistuoti bet kurioje molekulės vietoje. Kartais vienai molekulinei formulei gali būti kelios struktūros, keičiant kelių jungčių padėtį. Šios molekulės turi lokalizuotą elektronų sistemą.
Aromatiniai angliavandeniliai:
Aromatiniuose angliavandeniliuose jie turi alternatyvią viengubą ir dvigubą jungčių sistemą, kad sudarytų konjuguotų jungčių sistemą, kuri delokalizuoja kai kuriuos elektronus. (Delokalizuoti elektronai gali pereiti iš vienos jungties į kitą).
alifatinių ir aromatinių angliavandenilių reakcijos
Alifatiniai angliavandeniliai:
Sotieji angliavandeniliai patiria pakeitimo reakcijas; nesotieji angliavandeniliai pasiekia stabilumą pridėjimo reakcijos būdu. Tačiau kai kurios reakcijos vyksta kontroliuojamomis sąlygomis nenutraukiant kelių ryšių.
Aromatiniai angliavandeniliai:
Aromatiniai angliavandeniliai yra nesotieji, tačiau turi stabilią konjuguotų elektronų sistemą, todėl jie labiau linkę į pakeitimo, o ne sudėjimo reakcijas.
Vaizdo sutikimas: Inductiveload „Polycyclic Aromatic Hydrocarbons“- įkėlėjo, „Accelrys DS Visualizer“darbas. (Viešasis domenas) per Commons






